Guía para pacientes
Actualización 2025 – Basada en Bethesda 2023, ATA 2025 y Consenso ATA–ETA–EANM–SNMMI 2021
Autor: Dr. Ricardo Mendoza Guerrero — Medicina Interna, Endocrinología y Tiroidología
Versión: noviembre 2025 • Venezuela

📘 Índice
I. Introducción
II. Sistema de reporte Bethesda (2023)
III. Resultado Bethesda III
IV. Resultado Bethesda IV
V. Pruebas genéticas disponibles en Venezuela
VI. Cómo interpretar los resultados de las pruebas genéticas moleculares
VII. Elección de prueba genética y conducta según escenario
VIII. Aspectos logísticos y biéticos
IX. Conclusiones
X. Bibliografía
I. Introducción
🦋 ¿Qué es un nódulo tiroideo?
Un nódulo tiroideo es una pequeña masa o bulto que se forma dentro de la glándula tiroides. Es algo muy frecuente — hasta la mitad de las personas adultas tienen uno o más nódulos — y la mayoría son benignos, es decir, no cancerosos.
🔬 ¿Qué es una Punción de la tiroides (PAAF) y por qué se hace?
Cuando aparece un nódulo, la manera más segura de estudiarlo es mediante una punción por aspiración con aguja fina (PAAF).
Este procedimiento, rápido y ambulatorio, consiste en obtener una pequeña muestra de células del nódulo para analizarlas al microscopio.
El resultado de esa evaluación se clasifica con un sistema internacional llamado Bethesda, que tiene seis posibles categorías (de I a VI).
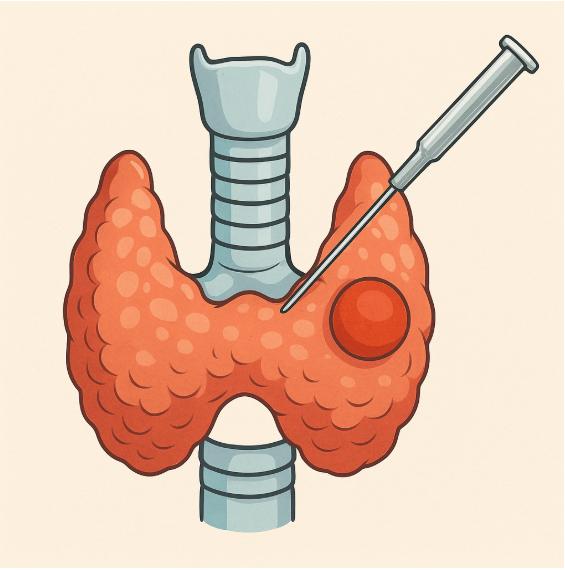
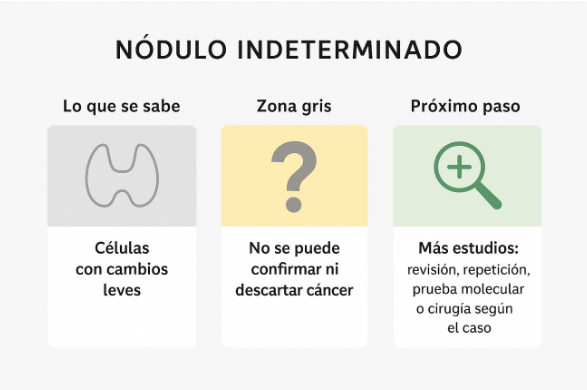
❓ ¿Qué significa que el resultado sea “indeterminado”?
A veces, las células no se ven completamente normales, pero tampoco muestran cambios suficientes para confirmar cáncer.
Cuando ocurre esa situación, el resultado se denomina “indeterminado”, y puede corresponder a dos categorías:
- Bethesda III: atipia o lesión folicular de significado indeterminado (AUS/FLUS)
- Bethesda IV: neoplasia folicular o sospechosa de neoplasia folicular (FN/SFN)
Tener un resultado indeterminado no significa tener cáncer, sino que las células no dan información definitiva.
En estos casos, el objetivo del endocrinólogo es refinar el diagnóstico para decidir con seguridad si el nódulo debe operarse o simplemente vigilarse.
II. El sistema Bethesda (2023)
El Bethesda System for Reporting Thyroid Cytopathology (TBSRTC) es el lenguaje común que usan los médicos y citopatólogos de todo el mundo para informar los resultados de una PAAF tiroidea.
La tercera edición (2023) actualizó los valores de riesgo y las recomendaciones clínicas con base en estudios genéticos recientes.
Categoría Bethesda | Significado general | Riesgo estimado de cáncer* |
|---|---|---|
I | Muestra insuficiente o no diagnóstica | ≈ 13 % |
II | Benigna (no cancerosa) | ≈ 2–3 % |
III | Atipia o lesión folicular de significado indeterminado (AUS/FLUS) | ≈ 10–30 % |
IV | Neoplasia folicular o sospechosa de neoplasia folicular (FN/SFN) | ≈ 25–40 % |
V | Sospechosa de malignidad | 65–80 % |
VI | Maligna (confirmada) | 98–99 % |
*Los porcentajes son promedios internacionales; pueden variar según la edad, los hallazgos ecográficos y los resultados de estudios moleculares.

El resultado Bethesda III o IV significa que el nódulo necesita una evaluación adicional, no que usted tenga cáncer.
Gracias a las pruebas genéticas moleculares modernas y a la experiencia clínica, más del 70 % de estos casos pueden evitar una cirugía innecesaria.
III. Cuando el resultado es Bethesda III (AUS/FLUS)
Atipia o lesión folicular de significado indeterminado

Su resultado indica que en la muestra obtenida por PAAF hay células que muestran algunos cambios, pero no los suficientes para asegurar si el nódulo es benigno o maligno.
Esto no es un diagnóstico de cáncer, sino una zona intermedia en la que el citopatólogo observa ciertas alteraciones leves, que pueden deberse a diversas causas:
- procesos inflamatorios (por ejemplo, tiroiditis)
- cambios en el crecimiento celular
- menos frecuentemente, una lesión tumoral folicular
Por eso se llama “de significado indeterminado”: las células se ven distintas, pero no claramente malignas.

Según el Sistema Bethesda (2023), el riesgo promedio de que un nódulo Bethesda III sea maligno está entre 10 y 30%.
Esto significa que:
- 7 a 9 de cada 10 nódulos Bethesda III son benignos.
- Solo 1 a 3 de cada 10 resultan finalmente cancerosos (generalmente tumores diferenciados y curables).
El riesgo puede ser un poco mayor si el nódulo presenta características sospechosas en la ecografía (como microcalcificaciones o márgenes irregulares), o si existen mutaciones genéticas de riesgo.


Cuando el resultado es indeterminado, no es necesario correr ni tomar decisiones inmediatas.
El siguiente paso depende de tres factores:
1️⃣ la calidad de la muestra
2️⃣ la apariencia del nódulo en ecografía
3️⃣ l la disponibilidad de pruebas genéticas moleculares.
A continuación se resumen las opciones más seguras y recomendadas:
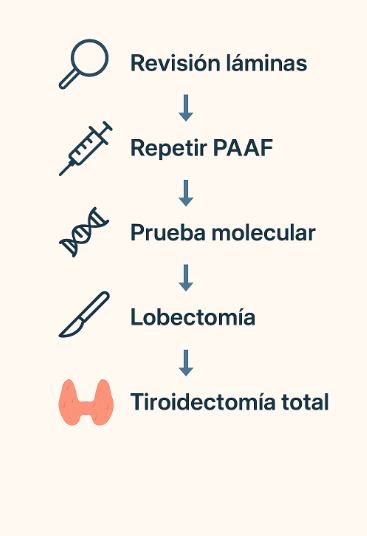
- Revisión experta de las láminas (segunda opinión)
El primer paso suele ser pedir que un citopatólogo con experiencia en tiroides revise la muestra.
Hasta el 40% de los casos Bethesda III pueden reclasificarse como benignos o diagnósticos al revisar las láminas originales.

- Repetir la punción de la tiroides (PAAF)
Si la muestra original tenía pocas células o resultó dudosa, puede repetirse la punción (habitualmente en 6–12 semanas).
Una segunda punción (PAAF) bien dirigida, con guía ecográfica, aclara el diagnóstico en la mayoría de los casos.
En aproximadamente la mitad de los pacientes, la repetición cambia el resultado a benigno, evitando procedimientos innecesarios.
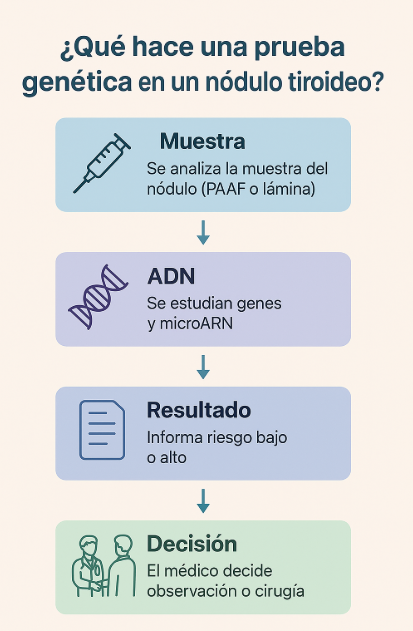
- Realizar una prueba genética molecular
Si el resultado sigue siendo indeterminado, el siguiente paso puede ser una prueba genética molecular, que analiza el material celular de su PAAF para buscar:
- mutaciones (cambios en los genes) o
- patrones de microARN (moléculas que indican si las células se comportan como benignas o malignas).
Estas pruebas ayudan a clasificar el riesgo real de su nódulo:
Resultado molecular | Significado clínico | Conducta sugerida |
|---|---|---|
Negativo / Benigno molecularmente | Muy bajo riesgo (≈1–5%) | Seguimiento y control ecográfico periódico. |
Moderado o Incierto | Riesgo intermedio | Decisión individualizada según edad, ecografía y preferencia del paciente. |
Positivo / Maligno molecularmente | Alto riesgo (>70%) | Cirugía recomendada (lobectomía o tiroidectomía parcial). |
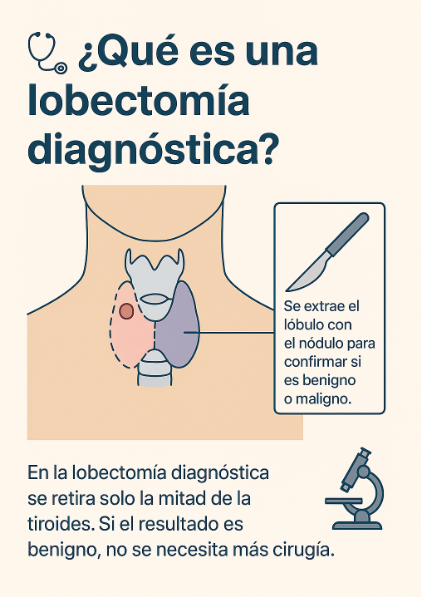
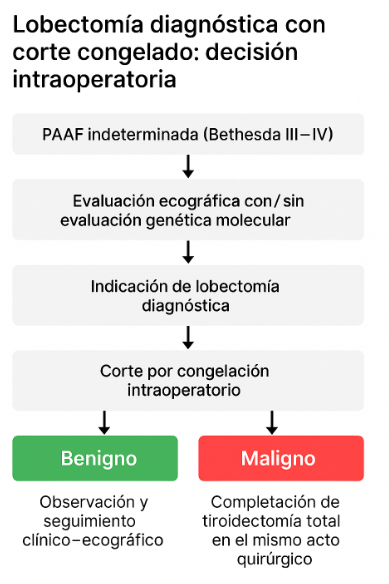
- Lobectomía diagnóstica
Si la prueba molecular no está disponible o el resultado es de alto riesgo, el médico puede recomendar una lobectomía diagnóstica — una cirugía limitada en la que se generalmente se extrae solo el lóbulo de la tiroides que contiene el nódulo.
Esto permite obtener el diagnóstico definitivo y, en la mayoría de los casos, no requiere tratamiento adicional si el resultado histológico es benigno.
Durante la operación, se analiza una pequeña muestra del tejido con una técnica rápida llamada corte por congelación.
Este estudio orienta la decisión en el mismo momento:
- Si el resultado es benigno, la cirugía se detiene y usted conserva la otra mitad de la tiroides.
- Si el resultado es maligno, el cirujano generalmente completa la tiroidectomía total (extirpar la otra mitad de la tiroides) durante la misma operación para garantizar el tratamiento completo.
En la mayoría de los casos, los nódulos resultan benignos, y la cirugía se limita a la lobectomía.
Este método evita intervenciones innecesarias y asegura un tratamiento adecuado cuando es necesario.
❤️ En resumen
- Un Bethesda III no significa cáncer, sino incertidumbre diagnóstica.
- En la mayoría de los casos, el nódulo es benigno.
- Su médico puede sugerir:
- Revisión de la muestra
- Repetir la punción
- O realizar una prueba molecular que defina el riesgo real.
- Solo en casos seleccionados se recomienda cirugía diagnóstica.
- El objetivo es evitar operaciones innecesarias y asegurar un manejo seguro, personalizado y con evidencia científica.
IV. Cuando el resultado es Bethesda IV (FN/SFN)
Neoplasia folicular o sospechosa de neoplasia folicular
🧠 ¿Qué significa un resultado Bethesda IV?
Su resultado indica que las células del nódulo forman un tumor de origen tiroideo.
Sin embargo, al microscopio no se puede saber con certeza si ese tumor es benigno (adenoma folicular) o maligno (carcinoma folicular), porque la diferencia solo puede confirmarse analizando el tejido completo, no solo las células sueltas.
👉 En otras palabras, el citólogo sospecha una neoplasia, pero la biopsia por PAAF no puede determinar su comportamiento.
📊 ¿Cuál es el riesgo real de cáncer?
Según la tercera edición del sistema Bethesda (2023), el riesgo promedio de malignidad para un nódulo Bethesda IV es de 25% a 40%.
En los casos con células oncocíticas (tipo Hürthle), el riesgo puede llegar hasta 45%.
Esto significa que:
- Más de la mitad de los nódulos Bethesda IV son benignos.
- 1 a 4 de cada 10 pueden corresponder a un tumor maligno, habitualmente bien diferenciado y con buen pronóstico.
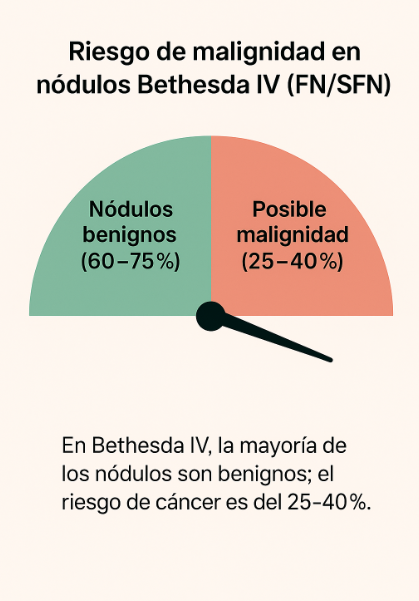

El resultado Bethesda IV no confirma cáncer, pero sí justifica una evaluación más profunda, porque el riesgo es mayor que en Bethesda III.
La conducta depende de los hallazgos clínicos, ecográficos y moleculares.
A continuación, se explican los pasos más importantes:
- Confirmación citológica (sin repetir la PAAF)
A diferencia del Bethesda III, no se recomienda repetir la punción, porque el patrón folicular suele mantenerse y una segunda muestra no aportará nueva información.
El objetivo ahora es complementar el diagnóstico con estudios moleculares o histológicos.
- Pruebas genéticas moleculares
Las pruebas genéticas o de microARN pueden identificar si el nódulo tiene mutaciones asociadas a cáncer o si, por el contrario, muestra un perfil benigno.
Resultado molecular | Significado clínico | Conducta sugerida |
|---|---|---|
Negativo / Benigno molecularmente | Riesgo muy bajo (<5%) | Seguimiento clínico y ecográfico. |
Positivo (mutaciones RAS, BRAF, TERT, RET, NTRK, etc.) | Riesgo alto (≈70–90%) | Cirugía recomendada (lobectomía o tiroidectomía total). |
Incierto / indeterminado | Depende de la clínica y ecografía | Decisión individualizada junto al endocrinólogo. |
Las pruebas genéticas moleculares no reemplazan la cirugía cuando el riesgo es alto, pero ayudan a evitar operaciones innecesarias en pacientes con perfil benigno.
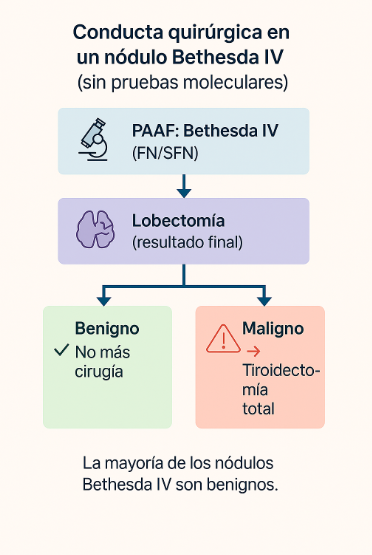
- Lobectomía diagnóstica
Si el resultado molecular no está disponible o es de alto riesgo, se recomienda una lobectomía diagnóstica, que consiste en extirpar el lóbulo de la tiroides donde se encuentra el nódulo.
- Si el estudio posterior demuestra que el nódulo era benigno, no se requiere más cirugía.
- Si resulta maligno, se decide junto al especialista si conviene completar la tiroidectomía o realizar seguimiento según el tipo de cáncer.
En la mayoría de los casos, la cirugía es curativa y segura, con mínima afectación hormonal.
⚖️ Decidir con calma y con información
Un resultado Bethesda IV puede causar preocupación, pero es importante recordar que:
- Más de la mitad de estos nódulos son benignos.
- Las pruebas genéticas moleculares ayudan a definir con precisión si es necesario operar.
- Cuando la cirugía es indicada, suele ser limitada (lobectomía) y con excelente pronóstico.
Su médico endocrinólogo valorará todos los factores (edad, tamaño del nódulo, ecografía, resultados moleculares y sus preferencias personales) antes de recomendar la mejor opción.
❤️ En resumen
- Bethesda IV significa “probable tumor folicular”, pero no necesariamente cáncer.
- El riesgo de malignidad es moderado (25–40%).
- No se repite la punción: se pasa a pruebas moleculares o cirugía diagnóstica.
- Si la prueba molecular es benigna → seguimiento.
- Si es de alto riesgo o no disponible → lobectomía diagnóstica.
- La gran mayoría de los pacientes con este resultado tienen curación completa y mantienen su función tiroidea normal.
V. Pruebas genéticas moleculares disponibles en Venezuela (2025)
🧬 ¿Qué son las pruebas genéticas moleculares?
Las pruebas genéticas moleculares tiroideas analizan el material genético (ADN, ARN o microARN) de las células obtenidas en la PAAF.
Su objetivo es determinar si el nódulo tiene características benignas o malignas, incluso cuando la citología es indeterminada (Bethesda III o IV).
Estas pruebas no reemplazan la evaluación médica ni la ecografía, pero aportan información muy valiosa para evitar cirugías innecesarias o, si el riesgo es alto, planificar la cirugía adecuada.
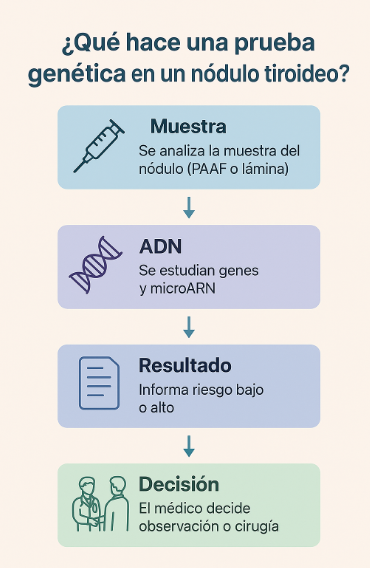
💡 ¿Por qué son útiles?
Porque cuando la citología no da una respuesta clara, las pruebas moleculares pueden:
- Confirmar que el nódulo es benigno, evitando una operación.
- Detectar mutaciones asociadas a cáncer, permitiendo actuar con rapidez.
- Definir la extensión quirúrgica más adecuada (por ejemplo, lobectomía parcial o total).
En resumen: ayudan a que la decisión médica sea más personalizada, segura y basada en evidencia.
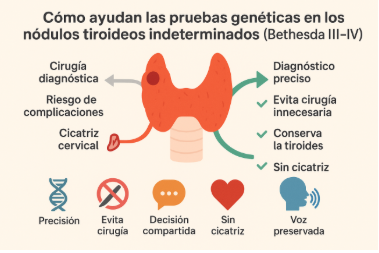

Representa el manejo tradicional sin prueba molecular:
- Cirugía diagnóstica como único método para confirmar el diagnóstico.
- Riesgo de complicaciones (daño al nervio que controla a las cuerdas vocales con afectación de la voz, hipocalcemia, necesidad de levotiroxina).
- Cicatriz en el cuello, consecuencia estética.


Representa el manejo con apoyo molecular (ThyGeNEXT–ThyraMIRv2, mir-THYpe, Afirma GSC):
- Diagnóstico preciso gracias al análisis genético y microARN.
- Evita cirugía innecesaria al confirmar benignidad molecular.
- Conserva la tiroides y su función hormonal.
- Sin cicatriz: el paciente evita una herida visible y las posibles secuelas estéticas, sobre la voz y el nivel del calcio en la sangre.


Cada ícono resume un beneficio clínico y humano clave:
Ícono | Significado |
|---|---|
| Precisión diagnóstica |
| Evita cirugía innecesaria |
| Decisión médica–paciente compartida |
| Sin cicatriz – bienestar y estética |
| Voz preservada – menor riesgo quirúrgico |
Las pruebas genéticas permiten diferenciar con precisión los nódulos tiroideos benignos de los malignos, evitando cirugías innecesarias.
Gracias a ellas, la mayoría de los pacientes con resultados indeterminados (Bethesda III–IV) pueden conservar su tiroides, evitar complicaciones y mantener un cuello sin cicatriz.
Son herramientas seguras, precisas y centradas en el bienestar del paciente.

Prueba molecular | Qué analiza | Muestra necesaria | Tiempo de entrega | Costo aproximado (USD) | Disponible en Venezuela | Ideal para | Comentarios |
|---|---|---|---|---|---|---|---|
ThyGeNEXT + ThyraMIRv2 (Interpace Diagnostics / VIDATEC Panamá) | ADN y ARN: busca mutaciones y analiza 10 microARN | Láminas citológicas hasta 5 meses de antigüedad o bloque celular | ~14 días hábiles | 3,531 (ambas) |
| Bethesda III y IV | Alta precisión; combina información genética y epigenética. Detecta mutaciones de alto riesgo como BRAF o TERT. |
mir-THYpe Full / pre-op (South Genetics) | MicroARN (y en versión pre-op: BRAF y TERT) | Láminas citológicas archivadas hasta 5 años | 20–25 días | 1,700 / 800 |
| Bethesda III y IV | No requiere nueva punción; ideal si las láminas están disponibles. Menor costo. |
Afirma GSC ± Xpression Atlas (Veracyte) | RNA-seq + inteligencia artificial; XA identifica mutaciones útiles para terapias dirigidas | Muestra fresca en medio especial (no lámina) | ~14 días | 2,500 |
| Bethesda III y IV | Prueba de alta calidad internacional, útil cuando se busca evitar cirugía; disponible solo en algunos países. |

- ThyGeNEXT / ThyraMIRv2: las láminas son válidas hasta 5 meses si están bien conservadas (secas, limpias y con suficiente celularidad).
- mir-THYpe: puede usar láminas archivadas hasta 5 años, incluso con diferentes tipos de tinción.
- Afirma GSC: requiere una muestra nueva en su medio específico, por lo que no puede realizarse con láminas anteriores.

Prueba | Ventajas | Desventajas |
|---|---|---|
ThyGeNEXT + ThyraMIRv2 | Máxima precisión; analiza tanto mutaciones como microARN; Permite distinguir lesiones de alto riesgo. | Mayor costo; requiere envío internacional y láminas recientes (≤5 meses). |
mir-THYpe | No necesita nueva punción; precio más accesible; resultados confiables en estudios latinoamericanos. | Menor capacidad de “confirmar cáncer” cuando es positivo; el resultado debe interpretarse junto con ecografía y clínica. |
Afirma GSC | Muy buen poder para descartar malignidad; incorpora análisis genómico avanzado. | No disponible comercialmente en Venezuela; requiere material fresco. |

La elección depende de la edad del paciente, la disponibilidad de láminas, el tiempo transcurrido desde la PAAF y las preferencias personales.
En general:
- Si las láminas son recientes (menos de 5 meses) y se desea máxima precisión → ThyGeNEXT + ThyraMIRv2.
- Si las láminas son antiguas (más de 5 meses) o no se desea repetir punción → mir-THYpe Full.
- Si existe acceso internacional y se busca una prueba de “regla-out” molecular → Afirma GSC (solo fuera del país).

- Las pruebas moleculares ayudan a tomar decisiones más seguras y personalizadas.
- En Venezuela, las opciones vigentes son ThyGeNEXT + ThyraMIRv2 y mir-THYpe.
- Cada prueba tiene ventajas y limitaciones, pero todas buscan evitar cirugías innecesarias.
- Su endocrinólogo lo orientará sobre cuál es la mejor opción según su caso, edad, ecografía y disponibilidad de muestra.
VI. Elección de prueba y conducta según el resultado Bethesda

Significado:
Las células del nódulo muestran cambios leves, pero no suficientes para saber si es benigno o maligno.
Riesgo promedio de cáncer:
Aproximadamente 10–30% (la mayoría son benignos).
Objetivo:
Evitar cirugías innecesarias y confirmar si realmente existe riesgo.

Paso | Qué se hace | Por qué es importante |
|---|---|---|
1️⃣ Revisión experta de láminas | Un citopatólogo especializado revisa nuevamente la muestra. | Hasta 4 de cada 10 casos pueden reclasificarse como benignos sin necesidad de repetir la punción. |
2️⃣ Repetir la PAAF (si es necesario) | Si la muestra fue pequeña o dudosa, se puede repetir con guía ecográfica. | En más del 50% de los casos, el segundo resultado aclara el diagnóstico. |
3️⃣ Prueba molecular | Si el resultado sigue siendo indeterminado, se analiza el ADN o microARN del nódulo. | Si el resultado molecular es benigno, el seguimiento suele ser suficiente. |
4️⃣ Cirugía (lobectomía diagnóstica) | Solo si la prueba molecular no está disponible, o si el riesgo es alto. | Permite diagnóstico definitivo y tratamiento en un solo procedimiento. |

- Si la prueba molecular es negativa (benigna) → seguimiento clínico y ecográfico.
- Si es positiva o de alto riesgo → cirugía diagnóstica (lobectomía).
- Si no hay acceso a pruebas → repetir la PAAF o considerar cirugía según la ecografía.







Significado:
El nódulo tiene un patrón celular que sugiere un tumor, pero la PAAF no puede definir si es benigno o maligno.
Riesgo promedio de cáncer:
Entre 25% y 40% (más de la mitad son benignos).
Objetivo:
Confirmar si se trata de una neoplasia benigna o un carcinoma bien diferenciado.

Paso | Qué se hace | Por qué se hace |
|---|---|---|
1️⃣ Confirmación citológica | Se revisa la muestra inicial; no se recomienda repetir la punción. | La repetición no cambia el diagnóstico y retrasa la decisión. |
2️⃣ Prueba molecular | Permite diferenciar tumores benignos de malignos antes de operar. | Si el resultado es negativo, se evita cirugía; si es positivo, se confirma necesidad quirúrgica. |
3️⃣ Lobectomía diagnóstica | Se extirpa el lóbulo donde está el nódulo. | Permite diagnóstico definitivo y, si es benigno, no se requiere más cirugía. |

- Si la prueba genética molecular es benigna o negativa → seguimiento clínico y ecográfico.
- Si es positiva o no disponible → cirugía diagnóstica (lobectomía).
- Si el resultado histológico posterior muestra cáncer → decidir extensión quirúrgica junto al especialista.

Resultado de la PAAF | Riesgo de cáncer | Primer paso | Segundo paso | Conducta final |
|---|---|---|---|---|
Bethesda III | 10–30% | Revisión de láminas y posible nueva PAAF | Prueba genética (si está disponible) | Seguimiento si benigno; cirugía si alto riesgo |
Bethesda IV | 25–40% | Confirmación del diagnóstico (sin repetir PAAF) | Prueba genética o lobectomía diagnóstica | Seguimiento si benigno; cirugía si maligno |

Recibir un resultado Bethesda III o IV no significa tener cáncer, sino que se necesitan más estudios para entender mejor su nódulo.
Hoy contamos con pruebas moleculares de alta precisión que reducen la necesidad de cirugía y permiten decisiones médicas seguras y personalizadas.
Su médico endocrinólogo lo acompañará paso a paso para:
- Analizar la citología y la ecografía
- Valorar si conviene una prueba molecular
- Definir el plan más adecuado para su caso

VII. Cómo interpretar los resultados de las pruebas moleculares
Las pruebas moleculares no entregan un resultado de “positivo o negativo para cáncer” como una biopsia tradicional.
Cada una usa su propia terminología y un algoritmo interpretativo que estima el riesgo de malignidad del nódulo tiroideo.
Por eso es importante que el médico endocrinólogo le ayude a entender su significado exacto.

Esta prueba combina dos análisis complementarios:
- ThyGeNEXT®: busca mutaciones y fusiones genéticas en los genes más comunes del cáncer de tiroides (RAS, BRAF, TERT, RET/PTC, NTRK, entre otros).
- ThyraMIRv2®: analiza el patrón de expresión de 10 microARN que actúan como “interruptores” del comportamiento celular.
Terminología del informe:
Resultado | Significado | Conducta recomendada |
|---|---|---|
ThyGeNEXT positivo (mutaciones de alto riesgo: BRAF, TERT, RET/PTC) | Alta probabilidad de cáncer o comportamiento agresivo | Cirugía (lobectomía o tiroidectomía). |
ThyGeNEXT con mutaciones leves (RAS, PTEN, etc.) | Riesgo intermedio; requiere ThyraMIRv2 para definir | Si ThyraMIRv2 es negativo → seguimiento. Si positivo → cirugía. |
ThyGeNEXT negativo + ThyraMIRv2 negativo | Riesgo residual muy bajo (≈1%) | No se recomienda cirugía; solo control ecográfico. |
ThyraMIRv2 positivo o moderado | Expresión molecular compatible con malignidad o lesión de riesgo | Evaluar cirugía según ecografía y contexto clínico. |


🧫 2. mir-THYpe (South Genetics)
Esta prueba mide la expresión de varios microARN, pequeñas moléculas que se comportan de forma diferente en los nódulos benignos y malignos.
Hay dos versiones:
- mir-THYpe Full: analiza la probabilidad de malignidad (positivo/negativo).
- mir-THYpe pre-operatorio: agrega marcadores pronósticos (BRAF, TERT, miR-146b) para planificar la extensión quirúrgica.
Terminología del informe:
Resultado | Significado | Conducta recomendada |
|---|---|---|
Negativo | Patrón molecular benigno. Riesgo de cáncer muy bajo (~4%). | Seguimiento clínico y ecográfico. |
Positivo | Patrón molecular maligno o sospechoso. Riesgo ~70–80%. | Cirugía diagnóstica o terapéutica según ecografía y tamaño del nódulo. |
💬 Un resultado negativo en mir-THYpe permite evitar cirugía en la mayoría de los pacientes; si es positivo, el pronóstico sigue siendo excelente tras cirugía.

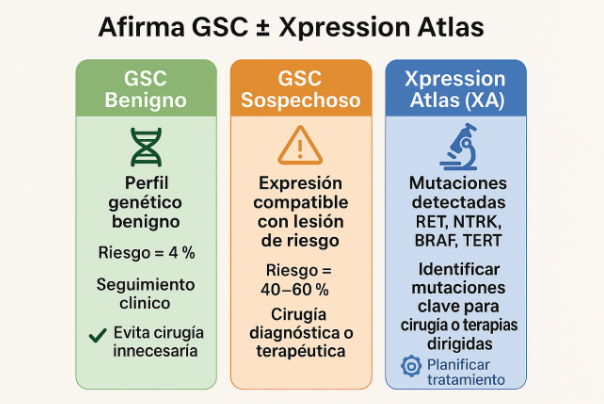
💻 3. Afirma GSC ± Xpression Atlas (Veracyte / South Genetics)
Esta prueba usa tecnología avanzada de RNA-secuenciación y algoritmos de inteligencia artificial.
Evalúa más de 1.000 genes para clasificar los nódulos indeterminados como “benignos” o “sospechosos”.
Terminología del informe:
Resultado | Significado | Conducta recomendada |
|---|---|---|
GSC Benigno | Patrón genético típico de nódulo no canceroso. ROM ~4%. | Seguimiento sin cirugía. |
GSC Sospechoso | Expresión genética compatible con lesión maligna o de riesgo. | Evaluar cirugía y solicitar análisis complementario (Xpression Atlas). |
Xpression Atlas (XA) | Identifica mutaciones o fusiones (RET, NTRK, BRAF, etc.) que pueden orientar terapias dirigidas o tipo de cirugía. | Se interpreta junto al endocrinólogo o cirujano. |
⚠️ Afirma GSC no está disponible actualmente en Venezuela, pero puede solicitarse en países vecinos a través de South Genetics.

Prueba | Cómo clasifica el resultado | Qué significa si es “benigno” | Qué significa si es “sospechoso / positivo” |
|---|---|---|---|
ThyGeNEXT + ThyraMIRv2 | Negativo / Moderado / Positivo | Muy bajo riesgo (≈1%) | Riesgo alto; se recomienda cirugía. |
mir-THYpe | Negativo / Positivo | Riesgo bajo (~4%) | Riesgo moderado–alto (~70%). |
Afirma GSC | Benigno / Sospechoso | Muy bajo riesgo (~4%) | Necesita XA o cirugía según contexto. |

- Léalo siempre acompañado de su médico.
Los resultados deben evaluarse junto con la ecografía y sus antecedentes. - Un resultado “negativo” no significa riesgo cero, pero sí implica una probabilidad muy baja.
- Un resultado “positivo” tampoco es un diagnóstico definitivo de cáncer, sino una señal de que se recomienda cirugía para confirmarlo.
- Las pruebas moleculares orientan decisiones, no reemplazan la clínica.

VIII. Aspectos logísticos y bioéticos

Durante la biopsia (PAAF), se obtienen pequeñas gotas de material celular del nódulo tiroideo.
Estas células se extienden sobre láminas de vidrio o se colocan en un líquido especial para su análisis microscópico.
Dependiendo del caso, esas mismas láminas pueden reutilizarse para las pruebas moleculares, si tienen suficiente material celular.

Cada prueba tiene sus propias condiciones y tiempos máximos de validez:
Tipo de muestra | Validez aproximada | Recomendaciones |
|---|---|---|
Láminas citológicas convencionales (usadas para ThyGeNEXT o ThyraMIR) | Hasta 5 meses desde la punción (según VIDATEC Panamá) | Guardarlas limpias, secas y protegidas de la humedad. Deben contener ≥80–300 células foliculares. |
Láminas para mir-THYpe | Hasta 5 años (según South Genetics) | Se aceptan láminas antiguas y diferentes tinciones (Papanicolaou, Diff-Quik, H&E). |
Bloques celulares (cell blocks) | Hasta 10 años | Útiles si la punción generó material abundante. |
Muestra líquida en preservante específico | 1–2 semanas a temperatura ambiente (6 meses refrigerada) | Solo si se hace una nueva PAAF destinada a la prueba. |


El transporte de las láminas o del bloque celular se realiza en envases especiales y sellados, con control de temperatura y trazabilidad.
Su médico o el laboratorio de origen (por ejemplo, VIDATEC o South Genetics) se encargan de la logística y del seguimiento del envío hasta el laboratorio central.

Prueba | Tiempo estimado | Forma de entrega |
|---|---|---|
ThyGeNEXT + ThyraMIRv2 | 14 días hábiles | Informe digital enviado al médico tratante y al paciente. |
mir-THYpe | 20–25 días | Informe electrónico con interpretación clínica. |
Afirma GSC | 14 días | Informe por correo electrónico (solo si se realiza fuera del país). |
El médico endocrinólogo revisa el informe junto con la historia clínica, ecografía y citología antes de explicarle el resultado final.

Prueba | Costo aproximado (USD) | Incluye análisis molecular y reporte clínico |
|---|---|---|
ThyGeNEXT + ThyraMIRv2 | 3,531 | Sí |
ThyGeNEXT solo | 1,712 | Sí |
ThyraMIRv2 solo | 2,140 | Sí |
mir-THYpe Full | 1,700 | Sí |
mir-THYpe pre-op | 800 | Sí |
Afirma GSC ± XA | 2,500 | No disponible actualmente en Venezuela |

Teléfonos de contacto:
- Vidatec Venezuela: 0412 2067787
- South Genetics Venezuela: 0424 1714761

Antes de realizar cualquier prueba molecular, el paciente debe autorizar por escrito el uso de su muestra para análisis genético.
El consentimiento informado incluye:
- Explicación del objetivo del estudio.
- Posibles resultados e implicaciones clínicas.
- Aclaratoria de que el resultado no es diagnóstico de cáncer, sino una estimación de riesgo.
- Confirmación de confidencialidad y protección de los datos personales.


Las pruebas moleculares se realizan en laboratorios certificados (CAP/CLIA) con estrictos protocolos de confidencialidad.
Los resultados solo se envían al médico tratante y al paciente autorizado, nunca a terceros sin consentimiento.

- Las láminas de la PAAF pueden aprovecharse para estudios moleculares, según su antigüedad y calidad.
- Cada prueba tiene tiempos de validez y transporte específicos.
- Los resultados tardan entre 2 y 3 semanas y siempre deben interpretarse junto al médico.
- Es fundamental leer y firmar el consentimiento informado antes del análisis.
- Toda la información se maneja con confidencialidad y ética profesional.

IX. Conclusiones finales

Recibir un resultado de citología “indeterminada” (Bethesda III o IV) puede generar preocupación, pero no significa que usted tenga cáncer.
En la mayoría de los casos, estos nódulos son benignos y solo requieren un seguimiento adecuado.
El objetivo de esta guía es ayudarle a comprender su resultado y las opciones que tiene para avanzar con seguridad y confianza.

Las pruebas genéticas modernas permiten analizar el comportamiento interno del nódulo, algo que antes no era posible con la citología tradicional.
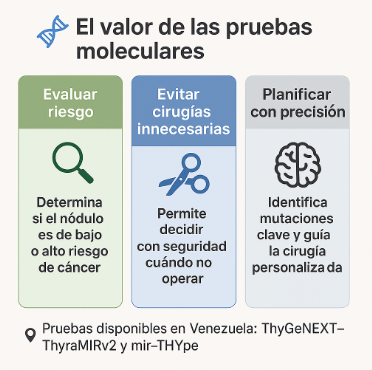
Gracias a estas herramientas, los médicos pueden:
- Determinar si el riesgo de cáncer es bajo o alto.
- Evitar cirugías innecesarias en la mayoría de los pacientes.
- Identificar mutaciones específicas cuando se requiere cirugía, mejorando la planificación quirúrgica.
En Venezuela, las pruebas ThyGeNEXT–ThyraMIRv2 y mir-THYpe ofrecen resultados confiables y seguros, con la asesoría de laboratorios certificados y el acompañamiento de su médico tratante.
🌍 En Venezuela (2025)
- Afirma GSC, aunque es una prueba excelente, no está disponible comercialmente.
- ThyGeNEXT + ThyraMIRv2 (VIDATEC Panamá) ofrecen el mayor detalle genético y epigenético.
- mir-THYpe (South Genetics) es una opción más accesible, que puede utilizar láminas antiguas hasta 5 años.
Ambas alternativas permiten reducir el número de cirugías innecesarias y brindar tranquilidad diagnóstica.
⚖️ Decisiones informadas, no apresuradas
Cada caso es único.
La decisión entre repetir la punción, hacer una prueba molecular o ir a cirugía diagnóstica debe tomarse considerando:
- La ecografía del nódulo
- La edad y los antecedentes del paciente
- La disponibilidad de la muestra
- Las preferencias personales
🩺 Lo más importante es que la decisión sea compartida, razonada y plenamente comprendida.
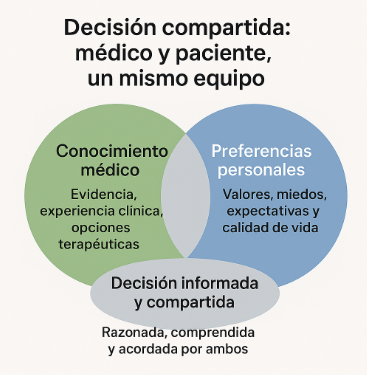
La toma de decisiones compartida es un proceso colaborativo en el que el médico y el paciente combinan la evidencia científica con las preferencias personales y valores individuales.
El objetivo es alcanzar una decisión razonada, comprendida y mutuamente acordada, asegurando que el paciente entienda las opciones, los riesgos y los beneficios de cada alternativa.
Este modelo fomenta la autonomía del paciente, mejora la adhesión terapéutica y fortalece la relación médico–paciente como alianza terapéutica.
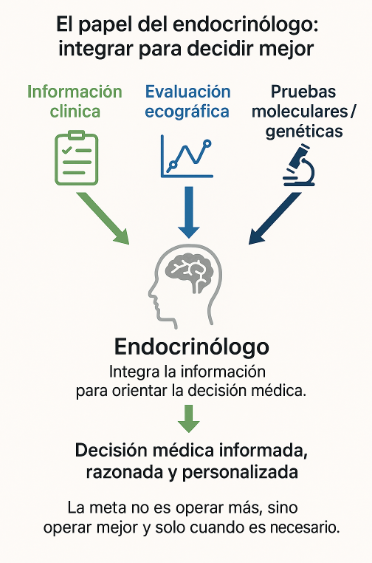
🧠 El papel del endocrinólogo
Su endocrinólogo no solo interpreta el resultado de la PAAF o de la prueba molecular:
también integra toda la información —clínica, ecográfica y genética— para ayudarle a tomar la mejor decisión médica posible.
La meta no es operar más, sino operar mejor y solo cuando sea necesario.

- Un resultado Bethesda III o IV no es un diagnóstico de cáncer.
- Más del 70% de los nódulos indeterminados son benignos.
- Las pruebas moleculares ayudan a diferenciar los casos que necesitan cirugía de los que no.
- Las cirugías diagnósticas actuales son seguras, curativas y de baja complejidad.
- Y lo más importante: usted no está solo en este proceso.
Su médico lo acompañará en cada paso, con información clara, evidencia científica y empatía.

X. Bibliografía
- Cibas ES, Ali SZ (eds.). The Bethesda System for Reporting Thyroid Cytopathology, 3rd ed. Springer; 2023.
- Haugen BR, et al. 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid. 2016; 26(1):1–133.
- Gulec SA, et al. ATA–ETA–EANM–SNMMI Joint Statement on Diagnostic and Theranostic Approaches in Thyroid Cancer. Thyroid. 2021.
- 2025 American Thyroid Association Management Guidelines for Adult Patients with Differentiated Thyroid Cancer. Matthew D. Ringel, et al. THYROID Volume 35, Number 8, 2025
- Interpace Diagnostics / VIDATEC Panamá. ThyGeNEXT–ThyraMIRv2: Technical Summary & Sample Reports. 2025.
- South Genetics. mir-THYpe Technical Brochure and Clinical Evidence. 2025.

Dr Ricardo Mendoza
Servicio de endocrinología
- Hospital Vargas de Caracas
- Tecnidiabetes
- Instituto Diagnóstico
Www.drricardomendoza.com
04140857871
IG: @doc.ricardomendoza




